微信在线咨询
微信在线咨询

| 产品编号 | 产品名称 | 产品包装 | 产品价格 |
| S0055 | 谷胱甘肽还原酶检测试剂盒(DTNB法) | 100次 | 515.00元 |
谷胱甘肽还原酶检测试剂盒(DTNB法)(Glutathione Reductase Assay Kit with DTNB)是一种简单易行的通过比色法来检测细胞、组织或其它样品中谷胱甘肽还原酶(Glutathione reductase,GR)活性的试剂盒。谷胱甘肽还原酶在许多组织中都有分布,可以维持细胞内充足的还原型谷胱甘肽(GSH)水平。GSH可以清除自由基和一些有机过氧化物,或作为谷胱甘肽氧化酶(Glutathione peroxidase)的底物来清除一些过氧化物。
谷胱甘肽还原酶可以还原氧化型谷胱甘肽(GSSG)生成还原型谷胱甘肽(GSH),而GSH可以和生色底物DTNB反应产生黄色的TNB和GSSG,并可以通过测定A412来检测TNB的生成量。适当设置应体系,前后两个反应合并起来后,GSSG/GSH过量而GR相对不足时,该反应体系中谷胱甘肽还原酶就成为整个反应体系的限速因素,此时黄色的TNB生成量和谷胱甘肽还原酶的活性呈线性正相关。从而通过测定A412就可以计算出谷胱甘肽还原酶的活性水平。本试剂盒的具体反应原理如下:
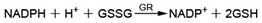

两个反应相合并:
 本试剂盒检测肝脏样品的检测效果如图1所示。图中可见,对于肝脏样品可以检测到比较强的谷胱甘肽还原酶的活性并且有很好的剂量效应。
本试剂盒检测肝脏样品的检测效果如图1所示。图中可见,对于肝脏样品可以检测到比较强的谷胱甘肽还原酶的活性并且有很好的剂量效应。
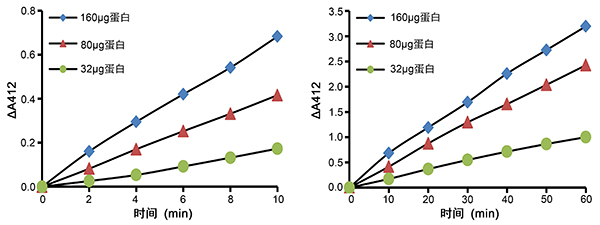 图1. 谷胱甘肽还原酶检测试剂盒(DTNB法)用于肝脏裂解样品的实测效果图。
包装清单:
图1. 谷胱甘肽还原酶检测试剂盒(DTNB法)用于肝脏裂解样品的实测效果图。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| S0055-1 | 谷胱甘肽还原酶检测缓冲液 | 50ml |
| S0055-2 | 样品稀释液 | 50ml |
| S0055-3 | NADPH | 5mg |
| S0055-4 | 氧化型谷胱甘肽(GSSG) | 14.2mg |
| S0055-5 | DTNB | 4.5mg |
| S0055-6 | DMSO | 1.5ml |
| — | 说明书 | 1份 |
保存条件:
-20℃保存,一年有效。NADPH溶解后宜分装并-70℃保存,4℃可以保存一天,-20℃保存一周后NADPH会降解10%以上。GSSG和DTNB在配制成溶液后,适当分装后-20℃保存。
注意事项:
本试剂盒检测时涉及氧化还原反应,因此所有氧化剂或还原剂都会干扰本试剂盒的测定。如果在样品中的还原剂无法避免,例如DTT、巯基乙醇等,则这些还原剂的总浓度至少低于0.1mM。0.15mM的DTT可以抑制40%的酶活力。另外,硫酸钠、硫酸铵和铁氰化物都会干扰本试剂盒的测定。请尽量避免。
样品可以立即测定,也可以-70℃冻存待以后测定。
一定要严格控制反应时的温度为25℃,否则会引起较多误差。
NADPH不太稳定,要严格按照后续说明操作,谨防失活。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:
1.样品的准备:
a.细胞样品的准备。对于贴壁细胞,由于后续用于酶活性的测定,应避免使用胰酶消化细胞,可以用PBS、HBSS或生理盐水洗涤一遍。对于悬浮细胞,可以离心收集细胞,并用PBS、HBSS或生理盐水洗涤一遍。后续可以用碧云天生产的Western及IP细胞裂解液(P0013)参考相应的说明裂解细胞样品。按照每100万细胞直接加入100-200微升裂解液的比例进行裂解。对于贴壁细胞,可以使用细胞铲或细胞刮(FLFT021/FSCP023/FSCP029)辅助收集细胞样品。如果出现裂解效果不佳的情况,可以把处在裂解液中的细胞样品用玻璃匀浆器在4℃或冰浴匀浆。随后4℃,12,000×g离心10分钟。取上清用于酶活性的测定。
b.组织样品的准备。动物用含有0.16mg/ml heparin的生理盐水(0.9% NaCl containing 0.16mg/ml heparin)灌流清除血液后获取组织样品。按照约每20mg组织加入200微升Western及IP细胞裂解液(P0013)或其它适当的匀浆液的比例,用TissueMaster™手持式组织研磨仪(E6600)或玻璃匀浆器在4℃或冰浴匀浆。4℃,12,000×g离心10分钟。取上清用于酶活性的测定。
c.红细胞裂解液的准备。用抗凝管收集血液,颠倒混匀。取至少500微升全血4℃ 2500×g离心5分钟。弃上清,用冰冷的约红细胞沉淀10倍体积的Western及IP细胞裂解液(P0013)或其它适当的匀浆液重悬沉淀,再同前离心,弃上清。加入约红细胞沉淀4倍体积的冰冷的Milli-Q级纯水裂解红细胞。12,000×g离心5分钟,取上清。
d.上述各种样品可以用碧云天生产的BCA蛋白浓度测定试剂盒(P0009/P0010/P0010S/P0011/P0012/P0012S)测定蛋白浓度。通常可以先取含1-100微克蛋白的样品用于谷胱甘肽还原酶的检测。注:对于GR活力较高的组织样品,含1-10微克蛋白的样品可能就能满足检测需求,而对于GR活力较低的样品,可能需要10-100微克的蛋白量。如果发现样品中谷胱甘肽还原酶的活力过高,可以用样品稀释液进行稀释。如果样品中谷胱甘肽还原酶的活力过低,则需适当加大蛋白用量。准备好的样品如果当日测定,可以在冰浴或4℃临时保存;如果不能当日检测,可以-70℃冻存。
2.试剂盒的准备工作:
a.配制6mM NADPH溶液的配制。在本试剂盒提供的5mg NADPH中加入1ml Milli-Q级纯水或重蒸水,溶解并混匀,即为6mM NADPH溶液。除立即待用部分外,其余的NADPH溶液需适当分装后尽快-70℃保存。
b.GSSG溶液的配制。在本试剂盒提供的14.2mg GSSG中加入10ml Milli-Q级纯水,溶解并混匀。除立即待用部分外,其余的GSSG溶液需适当分装后-20℃保存。
c.DTNB溶液的配制。在本试剂盒提供的4.5mg DTNB中加入1.5毫升本试剂盒提供的DMSO,溶解并混匀。除立即待用部分外,其余的DTNB溶液需适当分装后-20℃保存。
d.所有试剂在使用前均须在水浴中或PCR仪等设备上温育到25℃。
3.样品测定:
a.参考下表(表1),使用96孔板,依次加入各溶液,混匀。
|
|
空白对照 (blank) | 样品(sample) |
| GSSG溶液 | 100μl | 100μl |
| 谷胱甘肽还原酶检测缓冲液 | 90μl | 70-90μl |
| 样品 | 0μl | 0-20μl |
| NADPH溶液(6mM) | 10μl | 10μl |
| 总体积 | 200μl | 200μl |
b.加入6.6微升DTNB溶液,混匀。
c.立即使用适当的酶标仪或微量紫外分光光度计测定A412,此时记录为0分钟读值,即A412 (Time 0)。如果仪器可以设置温度,把温度设置在25℃,否则可以通过空调调节室温到25℃,待预计仪器也达到25℃后再开始测定A412。
d.每隔2分钟记录A412值,即A412 (Time n),至少连续记录10分钟,获得5个点的数据。或者如果仪器具备相应功能,可以让仪器连续测定10分钟或自动每隔2分钟测定一次A412。如果样品的吸光度比较低,可以延长孵育时间,样品的吸光度在一定范围内会随时间的延长接近于线性增加的,此时可以考虑每10分钟测定一次吸光度。
4.样品中谷胱甘肽还原酶酶活力的计算:
a.谷胱甘肽还原酶酶活力单位的定义:1个酶活力单位(1 unit)在25℃,pH7.5的条件下,在1分钟内可以还原化1微摩尔GSSG。1 U=1000 mU。
b.计算时每个样品的A412/min都需要扣除相应的样品本底对照测定出来的A412/min。测定出来的ΔA412/min最好能控制在0.005-0.1范围内。如测定出来的ΔA412/min数值过大,则可以把样品适当稀释或者减小样品的用量,如ΔA412/min数值过小,处理样品时需设法尽量浓缩样品、并适当加大样品的用量。肝脏裂解样品的实测效果参考图1。
注:ΔA412 (blank)=A412 (blank, Time n)-A412 (blank, Time 0);
ΔA412 (sample)=A412 (sample, Time n)-A412 (sample, Time 0);
ΔA412=ΔA412 (sample)-ΔA412 (blank);
ΔA412/min=ΔA412/n
c.对于谷胱甘肽还原酶:1mU/ml=1nmol TNB/min/ml=(ΔA412/min)/(εμM×L(cm))
即相当于:[检测体系中谷胱甘肽还原酶活力]= (ΔA412/min)/(εμM×L(cm))=[(ΔA412 (sample)-ΔA412 (blank))/min]/ (εμM×L(cm))
[样品中谷胱甘肽还原酶活力]=[检测体系中消耗谷胱甘肽还原酶活力]×[稀释倍数]/[样品中的蛋白浓度] = [(ΔA412/min)/(εμM×L(cm))]×[dil×(V(ml)/Vsample(ml))]/[样品中的蛋白浓度]
注:[检测体系中谷胱甘肽还原酶活力]的单位为mU/ml,[样品中的蛋白浓度]的单位为mg/ml,所以最终[样品中谷胱甘肽还原酶活力]的单位为:U/mg蛋白或mU/mg蛋白;
εμM为摩尔消光系数:TNB在A412的摩尔消光系数为0.01415μM-1cm-1;
L(cm)为测吸光度时的路径长度:200μl样品在一般的96孔中的高度约为0.552cm,如果使用不同的反应孔,请注意修改为溶液在该孔中的高度;
dil为样品的稀释倍数;
V(ml)为反应体系,本反应体系为0.2ml;
Vsample(ml)为反应体系中样品的体积,以毫升表示。
d.计算示例:样品的蛋白浓度经测定为5mg/ml,用样品稀释液稀释10倍后,取10微升稀释后的样品参考表1进行测定。如果ΔA412/min(sample)=0.048,ΔA412/min(blank)=0.006,那么:
[检测体系中谷胱甘肽还原酶活力]= (0.048-0.006)/(0.01415×0.552) =5.38mU/ml
[样品中谷胱甘肽还原酶活力]= 5.38mU/ml×10×0.2/0.01/(5mg/ml)= 0.2152U/mg(蛋白)









 微信在线咨询
微信在线咨询